Cho 6,485 gam hỗn hợp Ba và BaO vào nước dư thì thấy thoát ra 0,56 lít H2 (đktc)
A) viết các phản ứng xảy ra
B)tính phần trăm khối lượng mỗi chất trong hỗn hợp ban đầu
Câu 2. Cho 6,485 gam hỗn hợp A gồm Ba và BaO vào nước dư. Sau phản ứng, người ta thu được 0,56 lít khí H2 (đktc) và dung dịch B.
a. Tìm % khối lượng mỗi chất trong hỗn hợp đầu?
b. Tìm khối lượng chất tan trong dung dịch B?
Ba + 2H2O --> Ba(OH)2 + H2
BaO + H2O --> Ba(OH)2
nH2= 0.56/22.4=0.025 (mol)
=> nBa= 0.025 (mol)
mBa= 0.025*137=3.425g
mBaO= 6.485-3.425=3.06g
nBaO= 0.02 (mol)
%Ba= 3.425/6.485*100%= 52.81%
%BaO= 100 - 52.81= 47.19%
b) nBa(OH)2= 0.025+0.002= 0.045 (mol)
mBa(OH)2 = 0.045*171=7.695g
Cho 8,25 gam hỗn hợp kim loại Mg và Fe tác dụng hết với dung dịch HCL,thấy thoát ra 5,6 lít khí H2 (đktc)
a) Viết PTHH của phản ứng hoá học xảy ra
b) Tính khối lượng và thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp ban đầu
a. PTHH:
Fe + 2HCl ---> FeCl2 + H2 (1)
Mg + 2HCl ---> MgCl2 + H2 (2)
b. Gọi x, y lần lượt là số mol của Fe và Mg
Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PT(1): \(n_{H_2}=n_{Fe}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2}=n_{Mg}=y\left(mol\right)\)
\(\Rightarrow x+y=0,25\) (*)
Theo đề, ta lại có: 56x + 24y = 8,25 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}x+y=0,25\\56x+24y=8,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,07\\y\approx0,18\end{matrix}\right.\)
=> \(m_{Fe}=0,07.56=3,92\left(g\right)\)
=> \(\%_{m_{Fe}}=\dfrac{3,92}{8,25}.100\%=47,52\%\)
\(\%_{m_{Mg}}=100\%-47,52\%=52,48\%\)
A là hỗn hợp của Na, Mg, Al
- Cho a gam A vào nước dư phản ứng xong thoát ra 4,48 lít khí H2
- Cho a gam A vào dung dịch Ba(OH)2 dư thấy thoát ra 7,84 lít khí H2
- Cho a gam A vào dung dịch H2SO4 dư thoát ra 11,2 lít khí H2
Hãy tính a và phần trăm khối lượng của mỗi kim loại trong hỗn hợp ban đầu( biết thể tích các khí đo ở ĐKTC)
HD:
Thí nghiệm 1 chỉ có Na phản ứng:
Na + HOH \(\rightarrow\) NaOH + 1/2H2 (1)
0,4 0,2 mol
Thí nghiệm 2 chỉ có Al phản ứng (kim loại lưỡng tính):
Al + OH- + H2O \(\rightarrow\) AlO2- + 3/2H2 (2)
0,7/3 0,35 mol
Thí nghiệm 3 cả 3 chất đều phản ứng:
2Na + H2SO4 \(\rightarrow\) Na2SO4 + H2 (3)
Mg + H2SO4 \(\rightarrow\) MgSO4 + H2 (4)
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 (5)
Gọi x, y, z tương ứng là số mol của Na, Mg và Al trong a gam hh.
Ta có: x = 0,4 mol; z = 0,7/3 mol; x/2 + y + 3z/2 = 0,5. Suy ra: y = -0.5 < 0 (vô lí)
Bạn xem lại đề bài, đề bài ko đúng.
Do ở thí nghiệm 2 nH2 > n H2 thí nghiệm 1 -> ở thí nghiệm 1 NaOH hết ( Nếu NaOH dư thì nH2 ở 2 thí nghiệm đầu phải bằng nhau)
gọi a là số mol na b là số mol al c là số mol mg
Thí nghiệm 1 : Na+H20 - Naoh+1/2 H2
a a a/2
Al+naoh+h20-> naal02+3/2 H2
a 3/2a (do Naoh hết)
Vậy a/2+3/2 a = 0.2-> a=0.1
Thí nghiệm 2 : Na+h20 - naoh +1/2 H2
a a/2
Al+Oh-+h20--> alo2-+3/2 H2
b 3/2 b
a/2 +3/2 b = nH2=0.35-> b=0.2
Thí nghiệm 3: nH2 =0.5 = a/2+3/2b+c--> c =0.15
Vậy hh A gồm 0.1 Na 0.2 Al 0.15 Mg
Cho 9,6 gam hỗn hợp gồm Ca và CaO hòa tan hết vào nước, thu được 2,24 lít khí H 2 (đktc).
Viết phản ứng xảy ra.
Tính thành phần phần trăm theo khối lượng mỗi chất trong hỗn hợp ban đầu.
Tính khối lượng C a ( O H ) 2 thu được.
Cho 10,1 gam hỗn hợp Na, K tác dụng với nước dư, sau phản ứng thu được 3,36 lít khí H2 (đktc). (a) Viết phương trình phản ứng xảy ra. (b) Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
a 0,5a
\(2K+2H_2O\rightarrow2KOH+H_2|\)
2 2 2 1
b 0,5b
b) Gọi a là số mol của Na
b là số mol của K
\(m_{Na}+m_K=10,1\left(g\right)\)
⇒ \(n_{Na}.M_{Na}+n_K.M_K=10,1g\)
⇒ 23a + 39b = 10,1g (1)
Theo phương trình : 0,5a + 0,5b = 0,15(2)
Từ(1),(2), ta có hệ phương trình :
23a + 39b = 10,1g
0,5a + 0,5b = 0,15
⇒ \(\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
\(m_{Na}=0,1.23=2,3\left(g\right)\)
\(m_K=0,2.39=7,8\left(g\right)\)
0/0Na = \(\dfrac{2,3.100}{10,1}=22,77\)0/0
0/0K = \(\dfrac{7,8.100}{10,1}=77,23\)0/0
Hoà tan hoàn toàn 10,4 gam hỗn hợp gồm MgCo3 và MgO trong dung dịch axit sunfuric ( vừa đủ ).Thì thấy thoát ra 2,24 lít khí CO2 ( đktc ) a) Viết PTHH biểu diễn phản ứng xảy ra và tính phần trăm về khối lượng mỗi chất có trong hỗn hợp ban đầu . b) Tính khối lượng dung dịch axit sunfuric 9,8% đã dùng và nồng độ phần trăm của muối thu được sau phản ứng ( Cho : Mg=24,O=16,S=32,C=12,Ca=40,H=1,Cl=35.5)
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ a,PTHH:MgCO_3+H_2SO_4\rightarrow MgSO_4+H_2O+CO_2\uparrow\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\\ \Rightarrow n_{MgCO_3}=n_{CO_2}=0,1\left(mol\right)\\ \Rightarrow m_{MgCO_3}=0,1\cdot84=8,4\left(g\right)\\ \Rightarrow\%_{MgCO_3}=\dfrac{8,4}{10,4}\cdot100\%\approx80,77\%\\ \Rightarrow\%_{MgO}=100\%-80,77\%=19,23\%\)
\(b,m_{MgO}=10,4-8,4=2\left(g\right)\\ \Rightarrow n_{MgO}=\dfrac{2}{40}=0,05\left(mol\right)\\ \Rightarrow\sum n_{H_2SO_4}=n_{MgCO_3}+n_{MgO}=0,15\left(mol\right)\\ \Rightarrow\sum m_{H_2SO_4}=0,15\cdot98=14,7\left(g\right)\\ \Rightarrow\sum m_{dd_{H_2SO_4}}=\dfrac{14,7}{9,8\%}=150\left(g\right)\\ \sum n_{MgSO_4}=\sum n_{H_2SO_4}=0,15\left(mol\right)\\ \Rightarrow\sum m_{MgSO_4}=0,15\cdot120=18\left(g\right)\\ \Rightarrow C\%_{MgSO_4}=\dfrac{18}{10,4+150-0,1\cdot44}\approx11,54\%\)
Bài 7: Dẫn từ từ 6,72 lít hỗn hợp gồm CH4 và C2H2(đktc) lội qua dung dịch Brom dư thấy thoát ra 4,48 lít khí.
a) Viết PTHH xảy ra và tính phần trăm về khối lượng từng chất trong hỗn hợp ban đầu.
b) Tính khối lượng brom tham gia phản ứng
a)
PTHH: C2H2 + 2Br2 --> C2H2Br4
Khí thoát ra là CH4
\(n_{CH_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{C_2H_2}=\dfrac{6,72}{22,4}-0,2=0,1\left(mol\right)\)
\(\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,2.16}{0,2.16+0,1.26}.100\%=55,17\%\\\%m_{C_2H_2}=\dfrac{0,1.26}{0,2.16+0,1.26}.100\%=44,83\%\end{matrix}\right.\)
b)
PTHH: C2H2 + 2Br2 --> C2H2Br4
0,1--->0,2
=> mBr2 = 0,2.160 = 32 (g)
Cho 25 (gam) hỗn hợp gồm Nhôm và Đồng vào dung dịch H2SO4 loãng dư, sau phản ứng thấy thoát ra 5,6 (lít) khí H2 (ở đktc). Tính khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
nH2 = 5.6/22.4 = 0.25 (mol)
2Al + 3H2SO4 => Al2(SO4)3 + 3H2
1/6............................................0.25
mAl = 1/6 * 27 = 4.5 (g)
mCu = 25 - 4.5 = 20.5 (g)
Hòa tan hết 31,12 gam hỗn hợp X gồm Mg, Fe, Fe3O4, FeCO3 vào dung dịch hỗn hợp chứa H2SO4 và KNO3. Sau phản ứng thu được 4,48 lít hỗn hợp khí Y (đktc) gồm (CO2, NO, NO2, H2) có tỷ khối hơi so với H2 là 14,6 và dung dịch Z chỉ chứa các muối trung hòa với tổng khối lượng là m gam. Cho BaCl2 dư vào Z thấy xuất hiện 140,965 gam kết tủa trắng. Mặt khác, cho NaOH dư vào Z thì thấy có 1,085 mol NaOH phản ứng đồng thời xuất hiện 42,9 gam kết tủa và 0,56 lít khí (đktc) thoát ra. Các phản ứng xảy ra hoàn toàn.
Cho các kết luận sau:
(a) Giá trị của m là 82,285 gam.
(b) Số mol của KNO3 trong dung dịch ban đầu là 0,225 mol.
(c) Phần trăm khối lượng của FeCO3 trong hỗn hợp X là 18,638 .
(d) Số mol của Fe3O4 trong X là 0,05 mol.
(e) Số mol của Mg trong X là 0,15 mol.
Số kết luận không đúng là
A. 1.
B. 2
C. 3
D. 4
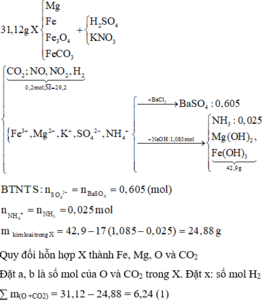

Từ (1), (2) và (3)
=> a = 0,28 (mol) ; b = 0,04 (mol) ; x = 0,06 (mol
=> m = 24,88 + 39 ( 0,255 –b –x) + 0,025.18 + 0,605.96 = 88, 285 => nhận định a) sai
nKNO3 = 0,225 – b – x = 0,125 => nhận định b) sai
%FeCO3 = ( 0,04.116/ 31,12).100% = 14,91% => nhận định c) sai
nO = 4nFe3O4 + nFeCO3 => nFe3O4 = 0,06 => nhận định d) sai
=> có tất cả 4 nhận định sai.